Fuente de imagen de dominio público pixabay

Fuente de imagen de dominio público pixabay
¿Pero era exclusiva del uranio esta propiedad? Marie Curie emprendió algunos experimentos con átomos de similar peso atómico. El óxido tórico producía una ionización que requería una carga piezoeléctrica de 53 x 10^-12 amperios para neutralizarla, esta propiedad no era exclusiva del uranio: el torio también era radiactivo.
Estos no fueron los únicos descubrimientos importantes de Marie Curie. Dos minerales de uranio, explica en su informe, <<son muchos más activos que el propio uranio, lo cual hace suponer que pueden contener un elemento aún más activo que el propio uranio>>. Por ejemplo, el mineral de uranio procedente de la pechblenda alcanzaba un registro cuatro veces mayor de lo que cabría esperar de la cantidad de uranio que contenía. No parecía haber explicarlo, a no ser que la pechblenda contuviera otro elemento radiactivo. Pero este tendría que estar presente en cantidades minúsculas, ya que de lo contrario ya se habría detectado. Además, tendrían que ser extremadamente radiactivo, a juzgar por los elevados que resultaban los registros de radiactividad en su conjunto. Como no se había encontrado ningún otro elemento que contuviera niveles de radiación similares, era probable que este fuera un elemento hasta entonces desconocidos.
Cita textual: Libro de Curie y la radiactividad por Paul Strathern, pág: 7. 2015.
Discutir de manera general de las radiaciones o en la temática de la radiactividad, hay que tener claro lo siguiente, que vivimos en un mundo naturalmente radioactivo, que proviene de fuentes naturales y artificiales en donde es inevitable exponerse a la mayoría de ellas. Y lo importante de todo esto con el tiempo se ha logrado y al mismo tiempo aprendido a utilizar la energía nuclear con diferentes propósitos: médicos, bélicos, industriales y para la generación de energía eléctrica partiendo como fuente de emisiones radiactivas.
Como nace esta interrogante de la radiactividad, para llegar a ella tenemos que saber, que la radiación es el transporte o la propagación de energía en forma de partículas u ondas. Les menciono también de manera dinámica, que la naturaleza de la radiactividad tenemos que tener en cuenta, lo que pasa dentro de los átomos, al mismo tiempo estos se conforman de tres tipos de partículas sub-atómicas: protones, neutrones y electrones, ya que la materia está constituida por átomos. Lo interesante ya que entramos en el mundo de los átomos, es que se debe conocer algo muy importante, como lo es una de sus condiciones en donde el átomo sea eléctricamente neutro, el cual se debe a que el núcleo de cada átomo contiene protones y neutrones rodeados por una nube de electrones, entonces imaginemos lo siguiente que los átomos tienen la misma cantidad de protones, que de electrones equilibrándose los unos con los otros, lo que hace que el átomo sea eléctricamente neutro. Lo que lo hace particularmente que el núcleo atómico tiene miles de veces más masa, que todos los electrones del átomo, en cuanto al diámetro del núcleo atómico es 10.000 veces más pequeño que el del átomo.
Ya teniendo claro un poco de conocimiento básico, ya podemos describir o decir de manera oportuna que el proceso de emisión se llama decaimiento, desintegración radioactiva o radiactividad, fíjense porque el principio mencione sobre la invencibilidad del espíritu humano, debido a todo el contexto científico, que se tuvo observar y determinar su fuente, en este caso la radiactividad y la forma en la esta se debe abordar. Cuando hablamos de ionización, se refiera a interacción que ocurre en un átomo o molécula y liberan un electrón, llegando hasta un punto que Las radiaciones ionizantes pueden llegar a ionizar o romper ligaduras en átomos o moléculas millones de veces antes de perder toda su energía, por eso se dice en la ciencia de la física de manera determinística, la radiactividad se aborda también como un fenómeno físico, que tiene propiedades muy particulares, relacionadas con la mecánica cuántica, debido a que se soporta según la siguiente abstracción de la realidad, es un proceso al azar o probabilístico, y la física únicamente puede predecir la frecuencia o el ritmo en que sucede, ya tenemos claro como es el manejo de este fenómeno a nivel de la ciencia de la física.
A nivel tecnológico en la aplicación del manejo de emisiones de radiactividad, debido a que se usa potencialmente la radiación electromagnética el cual está formada por partículas llamadas fotones. Este tipo de energía recibe diferentes nombres: luz visible, rayos X, rayos gamma, luz ultravioleta, microondas, teóricamente esta soportada en procesos atómicos que poseen energía suficiente como para ionizar átomos o moléculas, de tal manera que la actividad de un material que contiene radionucleidos es el número de desintegraciones, que ocurren por segundo en dicho material. Desde otra preceptiva también de las radiaciones ionizantes, existen las llamadas radiaciones no ionizantes, constituidas por ejemplo por la radiación infrarroja, gran parte del rango ultravioleta (UV), la luz visible, las ondas de radio, las microondas, la radiación empleada en las resonancias magnéticas.
Cierro con los siguientes fundamentos en radiación:
• Radiación α (alfa): en este tipo de caso tenemos un núcleo inestable emite un núcleo de helio; el núcleo original se transforma en otro, esto ocurre por lo siguiente, como resultado de la pérdida de dos protones el átomo cambiará a un elemento diferente, que tiene un número atómico dos valores hacia abajo, de tal manera que se considera o tiene lugar normalmente en los elementos pesados.
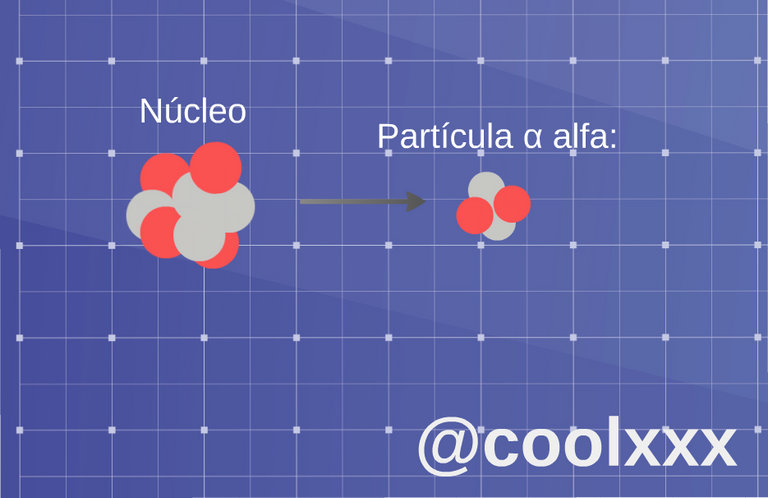
Radiación α (alfa).(Imagen elaborada por @coolxxx)
• Radiación β (beta): cuando llegamos a este caso existen dos vertientes de esta radiación: si un núcleo inestable emite un electrón de beta menos (β-), y si emite un positrón se denomina beta más (β+); también ocurre el caso, en el que núcleo original se transforma en otro de la siguiente manera, el átomo se convierte en un elemento un número más alto o más bajo en la serie progresiva.
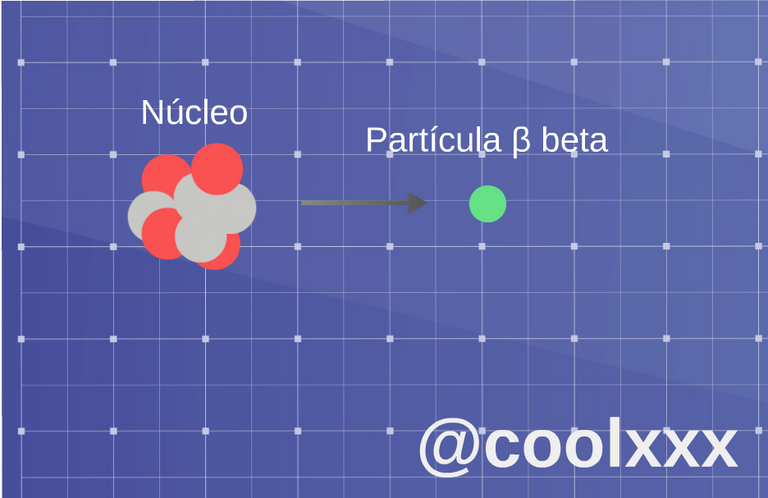
Radiación β (beta).(Imagen elaborada por @coolxxx)
• Radiación (gamma): en esta oportunidad tenemos que ahora son fotones usualmente de muy alta energía, emitidos por núcleos inestables u otros procesos y su núcleo únicamente pierde energía, en forma de radiación electromagnética, como lo son los rayos X o las microondas.
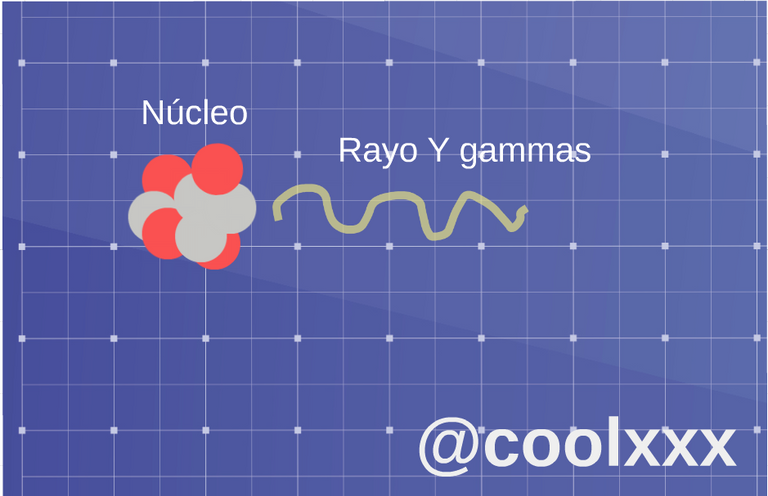
Radiación (gamma).(Imagen elaborada por @coolxxx)
Estos diferentes tipos de radiación reaccionan con la materia de diferentes maneras y algunas son mas penetrantes que otras.
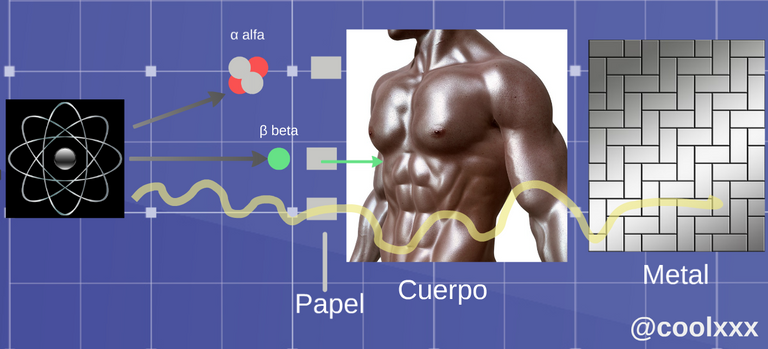
Penetración de los distintos tipos de radiación (Imagen elaborada y editada por @coolxxx)
Conclusión.
Es importante conocer y difundir que la radiactividad proviene de fuentes naturales y artificiales, tiene diversas aplicaciones tecnológicas, en la medicina, energía eléctrica nivel químico también porque todos los átomos de un mismo elemento químico, tiene la misma cantidad de protones. Esto es conocido como el número atómico del elemento y se lo denomina con la letra Z, también por un lado sabemos que todo lo que nos rodea es materia, la cual está compuesta por átomos.
Bibliografía consultada:
Tejera, A., "Energía nuclear: producción de radisótopos y electricidad", Ciencia y Desarrollo 23, p. 59, 1978
Folsing, U., Mujeres premio Nobel, Capítulo 1. Madrid: Alianza Editorial, 1992.
Muñoz Páez, A., Marie Curie, la radioactividad y los elementos. Barcelona: Colección Grandes Ideas de la Ciencia, RBA, 2013.
Quinn, S., Marie Curie, a life. Londres: Mandarin Paperbacks, 1995.
Radvanyi, P., Les Curie. París: Editions Belin, 2005.
Reid, R., , Marie Curie. Barcelona: Salvat Editores, 1987.
Strathen, P., Curie y la radioactividad. Madrid: Siglo XXI Editores, 1999.
Sánchez Ron, J. M., Marie Curie y su tiempo. Barcelona: Ed. Crítica, 2000.
Radiactividad y medio ambiente por León Garzón Ruipérez 1979.
La radiactividad Silvia Bulbulian. 2001.
Curie y la radiactividad por Paul Strathern. 2015.
